Среди множества вариантов аутоиммунных нарушений отдельное место занимает так называемый антисинтетазный синдром – заболевание, поражающее различные группы скелетных мышц. В журнале Case Report in Rheumatology был описан сложный случай антисинтетазного синдрома (АСС), ассоциированного с полимиозитом и поражением легких. Несмотря на дополнительные диагностические затруднения в виде ТЭЛА и неинфекционного эндокардита удалось своевременно выявить АСС и назначить необходимое лечение.
Описание клинического случая
59-летний мужчина обратился в клинику по месту жительства с жалобами на прогрессирующее и болезненное окрашивание кончиков пальцев в фиолетовый цвет, которое развилось в течение недели. Ему был поставлен диагноз синдрома Рейно, и через несколько дней к синюшному окрашиванию кончиков пальцев на фоне усиливающейся боли присоединился непродуктивный кашель. Пациент был госпитализирован в местную больницу, где ему была проведена КТ-ангиография грудной клетки, показавшая признаки септической эмболии легких. С помощью трансэзофагеальной эхокардиографии были обнаружены вегетации на митральном и легочном клапанах, но двукратные посевы крови были отрицательными. Пациенту был поставлен диагноз небактериального (марантического) эндокардита и назначен 2-хнедельный курс цефтриаксона. Он был выписан, но через 2 недели вернулся с персистирующей ишемией кончиков пальцев, прогрессирующей одышкой и легким кашлем. Повторная КТ-ангиография грудной клетки выявила тромбоэмболию легочной артерии, поэтому ему начали вводить гепарин внутривенно и перевели в другую клинику для обследования.
При поступлении в другое медицинское учреждение пациент был ориентирован и не испытывал дискомфорта. У него была нормальные показатели температуры тела и АД с ЧСС 100 уд/мин, ЧДД 20/мин и сатурацией 95% (с учетом назальной оксигенации). Также у него не было лимфаденопатии, тоны сердца были регулярными, без шумов. При аускультации были обнаружены хрипы в обоих легких. Осмотр брюшной полости не показал никаких отклонений. При осмотре конечностей были заметны ишемические изменения на кончиках пальцев с сохранением мышечной силы.
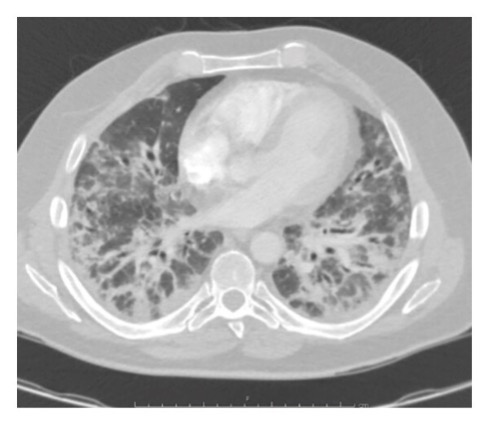
В течение 1-й недели госпитализации у пациента появилась слабость дельтовидной мышцы, из-за чего ему потребовалась помощь при движении. К 3-й неделе у него развилась орофарингеальная дисфагия и был установлен назогастральный зонд. На 7-й неделе госпитализации появилась прогрессирующая дыхательная недостаточность и понадобилась неинвазивная вентиляция легких. КТ грудной клетки с внутривенным контрастом показала правостороннюю легочную эмболию и инфаркты легких, а также двусторонние неоднородные затемнения и затемнения по типу матового стекла (рис. 1).
Рисунок 1. КТ-изображение грудной клетки, показывающее двустороннее затемнение и затемнения по типу «матового стекла».
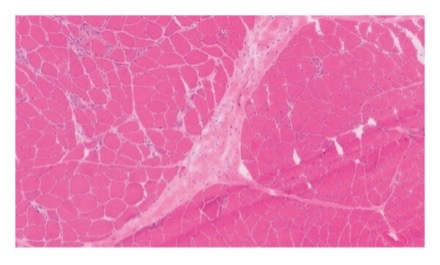
На чреспищеводной ЭхоКГ была обнаружена вегетация легочного клапана неопределенных размеров и вегетация митрального клапана 8×4 мм. Посевы крови и тестирование на ВИЧ были отрицательными. Посевы бронхоальвеолярного лаважа на наличие бактерий и грибков также были отрицательными, а результаты трансбронхиальной биопсии соответствовали организующейся пневмонии без патогенов. Такие лабораторные анализы, как определение фактора Лейдена и мутаций в гене протромбина, волчаночного антикоагулянта, антител к кардиолипину и бета-2-гликопротеину, ревматологические тесты, определение антител к вирусным гепатитам, показали отрицательный результат. Электрофорез белков сыворотки также не показал наличие М-белка, но было обнаружено повышение уровней креатинкиназы до 6284 ед/л, альдолазы – до 82 ед/л. МРТ правой ноги показала Т2-гиперинтенсивный сигнал в четырехглавой, приводящей, полуперепончатой и полусухожильной мышцах с усилением сигнала после введения контраста (признаки миозита). Результаты электромиографии левой руки соответствовали миопатическому процессу с расщеплением мышечных волокон, мионекрозом и нестабильностью мембран. Биопсия правого бицепса обнаружила некротизирующую миопатию без признаков воспаления (рис. 2).
Рисунок 2. Образец ткани правой двуглавой мышцы плеча с окраской гематоксилином и эозином, показывающая некротизирующую миопатию с некрозом мышечных волокон и регенерацией без воспаления.
Для уточнения диагноза был проведен иммуноблотинг, которая дал положительный результат на миозит-специфичные OJ-антитела к изолейцил-тРНК-синтетазе. В итоге пациенту был поставлен диагноз антисинтетазного синдрома на фоне тяжелого миозита и интерстициального заболевания легких с организующейся пневмонией.
После исключения инфекции пациенту были отменены антибиотики. Для лечения легочной эмболии были назначены антикоагулянты, организующейся пневмонии – метилпреднизолон 60 мг внутривенно каждые 6 часов в течение 3 дней, затем преднизон 40 мг 2 раза в день. Из-за прогрессирования миозита и слабости были возобновлены высокие дозы метилпреднизолона (1000 мг ежедневно в течение 5 дней), а по мере развития орофарингеальной дисфагии был начат четырехдневный курс внутривенного иммуноглобулина с постепенным снижением дозы преднизона. По причине низкого уровня тиопуринметилтрансферазы (ТПМТ) был назначен не азатиоприн, микофенолата мофетил 500 мг 2 раза в день. Мышечная слабость у пациента постепенно уменьшилась, и он, пройдя курс физиотерапии, вернулся домой в общей сложности через 5 месяцев после первого обращения.
Выводы авторов
АСС – тяжелое аутоиммунное нарушение, которое может проявляться по-разному в зависимости от присутствующих специфических аутоантител. У данного пациента первоначальный диагностический поиск в отношении инфекции, ревматологических и гематологических нарушений не позволил определить диагноз. Прогрессирующая мышечная слабость и положительный результат теста на антитела OJ к изолейцил-тРНК-синтетазе легли в основу диагностики АСС OJ на фоне миозита и интерстициального заболевания легких (ИЗЛ) с организующейся пневмонией. В подобных случаях необходим междисциплинарный подход к лечению с участием ревматолога и пульмонолога. У таких пациентов рекомендован контроль ИЗЛ с помощью легочных функциональных тестов каждые 3–6 месяцев и КТ грудной клетки высокого разрешения каждые 6–12 месяцев. Пациенты с прогрессирующим ИЗЛ, рефрактерным к иммуносупрессивной терапии, нуждаются в направлении на трансплантацию легких.
Справочная информация
Антисинтетазный синдром (АСС) – редкое и сложное аутоиммунное заболевание, которое относится к группе идиопатических воспалительных миопатий (ИВМ). АСС обычно имеет признаки полимиозита/дерматомиозита и сопровождается наличием аутоантител против фермента аминоацил-тРНК-синтетазы, которая играет решающую роль в синтезе белка. К этой группе антител относят анти-Jo-1, анти-PL-7, анти-PL-12, анти-OJ, анти-EJ, анти-KS, анти-ZO и другие. Наиболее часто встречаются случаи АСС, ассоциированного с анти-Jo-1.
АСС может проявляться в виде миозита, ИЗЛ, артрита, синдрома Рейно, гиперкератотических изменений кожи ладоней («руки механика») и лихорадки. Официальные диагностические критерии АСС, предложенные Connors et al. в 2010 году, требуют наличия антител к антиаминоацил тРНК-синтетазе в дополнение к одному или нескольким перечисленным симптомам. Более строгие критерии Solomon et al. (2011 г.) определяют обязательное наличие антител к антиаминоацил тРНК-синтетазе в дополнение к двум основным (полимиозит/дерматомиозит и ИЗЛ) или одному основному и двум дополнительным (синдром Рейно, артрит, «руки механика») симптомам.
Диагностика АСС включает определение высокоспецифичных к миозиту антител, уровней креатинкиназы и альдолазы, проведение КТ грудной клетки, МРТ и биопсии пораженных мышц. С целью лечения назначают кортикостероиды и другие иммунодепрессанты (азатиоприн, микофенолата мофетил, такролимус, ритуксимаб и циклофосфамид).
Источник: Vege A, Beery J, Kara A. Antisynthetase Syndrome in a Patient with Pulmonary Embolism and Nonbacterial Thrombotic Endocarditis. Case Rep Rheumatol. 2023 Jan 31;2023:9068597. doi: 10.1155/2023/9068597. PMID: 36760807; PMCID: PMC9904917.